Bioéconomie Temps de lecture 2 min
Les cellules ne gaspillent pas leurs ressources nutritionnelles, elles s’adaptent
Des scientifiques du laboratoire Toulouse Biotechnology Institute (TBI - INRAE-INSA Toulouse-CNRS) du centre INRAE Occitanie-Toulouse viennent de percer le fonctionnement du débordement métabolique. Ce qui semblait être un gaspillage des ressources par les cellules animales, les levures et les bactéries, se révèle être une stratégie d’adaptation.
Publié le 14 janvier 2026
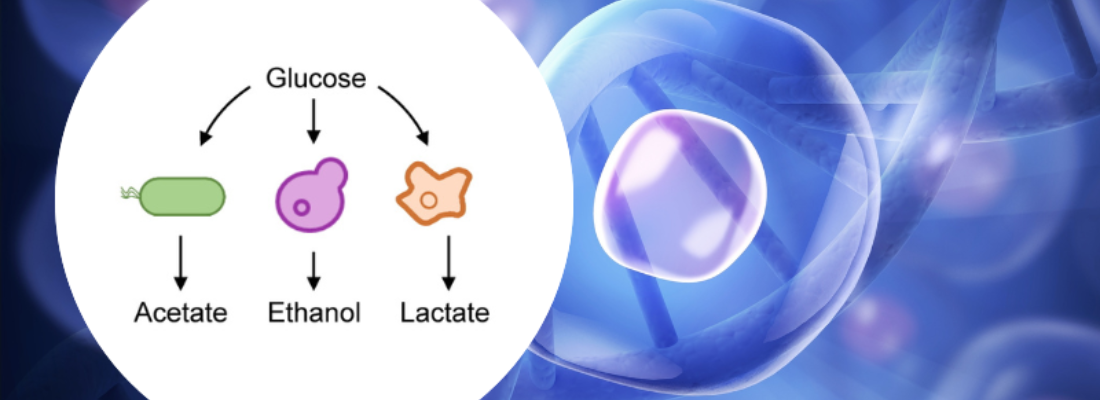
Les cellules animales, bactéries ou levures n’utilisent pas entièrement les nutriments qu’elles consomment pour leurs besoins en énergie ou leur multiplication. Elles rejettent une partie de ces ressources sous forme de sous-produits, qui peuvent sembler inutiles, voire toxiques. Appelé métabolisme Overflow ou débordement métabolique, ce phénomène, qui à première vue semble contreproductif, intriguait les biologistes depuis plus d’un siècle. Des scientifiques de TBI ont montré qu’il ne s’agit ni d’une faiblesse, ni d’une erreur mais d’une stratégie adaptative, commune aux bactéries, levures et cellules animales.
« L’évolution a optimisé les cellules pour leur efficacité mais aussi pour leur adaptabilité, souligne Pierre Millard, chercheur INRAE. Ce qui peut sembler un gâchis à court terme se révèle être un avantage de survie dans le long terme ».
Les molécules que rejettent les cellules ne sont pas seulement des déchets puisqu’ils peuvent aussi agir en tant que nutriments, messagers, et régulateurs. L’acétate aide les bactéries à gérer les perturbations nutritionnelles. L’éthanol soutient la production d’énergie chez les levures. Le lactate sert de carburant alternatif aux muscles et au cerveau chez l’humain.
Des principes communs
L’équipe de recherche a montré que le débordement métabolique avait un rôle important et qu’il était régi par des principes communs à toutes les cellules, des bactéries aux humains. Le premier est que ce processus est réversible et que les sous-produits peuvent être réutilisés. Il est déterminé par les interactions entre les grandes voies métaboliques. Sous contrôle partagé, ce phénomène résulte d’un équilibre entre la glycolyse, qui dégrade les sucres, le cycle de Krebs, qui les convertit en énergie, et les voies de débordement.
Le débordement métabolique est aussi soumis à des contraintes thermodynamiques. L’accumulation de sous-produits peut inverser les flux et pousser les cellules à les consommer en même temps que les sucres. Les sous-produits deviennent alors des nutriments. Ce phénomène joue un rôle dans l’adaptation en conférant de la résilience aux cellules face à des difficultés. L’acétate aide les bactéries à gérer les variations de disponibilité en sucre. L’éthanol fournit une source d’énergie de secours aux levures. Le lactate permet aux cellules animales d’échanger de l’énergie. « Pour l’adaptation, il vaut mieux perdre un peu d’efficacité à court terme mais gagner en flexibilité et en robustesse », estime Pierre Millard.
La compréhension du débordement métabolique ouvre la voie est des applications concrètes. Par exemple, il sera possible de développer des bioprocédés plus efficaces et plus résilients, pour la production de médicaments ou de biocarburant en minimisant la production de sous-produits ou en les recyclant en composés à haute valeur ajoutée. En santé, cette avancé aidera à mieux comprendre les pathologies liées à ce métabolisme, le rôle du lactate dans l’immunité ou le cancer.
Référence :
Thomas Gosselin-Monplaisir, Brice Enjalbert, Sandrine Uttenweiler-Joseph, Jean-Charles Portais, Stéphanie Heux, and Pierre Millard (2025). Overflow metabolism in bacterial, yeast, and mammalian cells: different names, same game . Mol Syst Biol, DOI : https://doi.org/10.1038/s44320-025-00145-x
