Alimentation, santé globale Temps de lecture 2 min
AvBD11, une protéine naturelle de l’œuf au potentiel thérapeutique prometteur
Publié le 10 janvier 2020

L’oeuf de poule contient près d’une centaine de molécules susceptibles de participer à la protection de l’œuf. Parmi celles-ci, on retrouve des peptides antimicrobiens appartenant à la famille des β-défensines, dont la β-défensine aviaire de type 11 (AvBD11), retrouvée dans l’œuf. Des résultats antérieurs publiés par l’une des équipes du consortium4 avaient démontré que cette protéine avait une activité antimicrobienne contre plusieurs souches bactériennes. Des analyses préliminaires de sa séquence protéique avaient mis en évidence sa taille atypique comparativement aux autres membres de cette famille, et laissaient présager la présence de deux domaines5de type « β défensines » (alors que les autres β-défensines ne possèdent qu’un seul domaine).
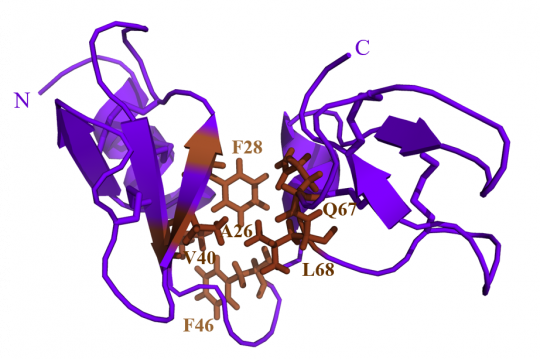
La résolution par résonance magnétique nucléaire de la structure de l’AvBD11 purifiée à partir de l’œuf révèle que cette protéine se présente effectivement sous la forme d’une structure compacte composée de deux domaines β-défensines associés. Cette caractéristique structurale, encore jamais décrite, nous permet de proposer ce peptide comme l'archétype d'une nouvelle famille structurale appelée « double-β-défensines aviaires (Av-DBD) ». Les deux domaines correspondants ont été produits individuellement par synthèse chimique et leurs activités testées, seules ou en synergie, afin d’évaluer leur contribution respective dans l’activité biologique de l’AvBD11. Les résultats révèlent le rôle décisif du premier domaine dans les activités antibactériennes, antiparasitaires et anti-invasives. En revanche, les activités antivirale et cytotoxique ne sont observées que pour le peptide entier, ce qui souligne l’importance de la complémentarité des deux domaines pour certaines activités.
L’AvBD11 est une protéine aux activités multiples, essentielles au développement embryonnaire de l’oiseau et qui possède très probablement d’autres activités encore méconnues. Outre son intérêt en biologie développementale et évolutive, de telles activités biologiques portées par l’AvBD11 sont potentiellement valorisables en santé humaine pour le développement d’agents thérapeutiques polyvalents capables de cibler des maladies d’origine infectieuse et des dérèglements cellulaires associés au cancer (demande de brevet en cours).
1 Ce travail a été réalisé dans le cadre de deux projets financés par la région Centre Val de Loire, « MUSE » (Medicinal USe of Eggs », 2014-00094512) coordonné par S. Réhault-Godbert et « SAPhyR-11 » (Structure/Activity and PHYlogenetic Relationships of AvBD11, 2017-119983) coordonné par N. Guyot. Le projet MUSE portait sur la caractérisation structurale et fonctionnelle de protéines et peptides purifiés à partir de l’œuf et sur l’évaluation de leur potentiel de valorisation en Santé Humaine/Animale. Ce projet avait permis la mise en évidence d’un peptide particulièrement prometteur, l’AvBD11, qui a fait l’objet d’une étude plus spécifique dans le projet SAPhyR-11.
2 Membrane protéique qui englobe le jaune
3Se dit d’une activité limitant la migration de cellules à travers un substrat, ce qui permet de contrôler leur dissémination dans un tissu ou un organisme
4Purification and characterization of avian beta-defensin 11, an antimicrobial peptide of the hen egg. Hervé-Grépinet et al. Antimicrob Agents Chemother doi: 10.1128/AAC.00204-10.
5Partie d’une protéine constituant une unité de base structurale et fonctionnelle
|
Références Structure, function and evolution of Gga-AvBD11, the archetype of a new structural avian-double-β-defensin family, Guyot et al., Proceedings of the National Academy of Sciences, doi: 10.1073/pnas.1912941117 Demande de brevet FR18 57411 du 9/08/2018 et PCT/EP2019/071388 « PEPTIDES DERIVES D'UNE BETA-DEFENSINE 11 AVIAIRE ET LEURS UTILISATIONS » |
