Dossier revue
Changement climatique et risquesLutter contre l'antibiorésistance
Publié le 17 juillet 2024

L’antibiorésistance, lorsque les bactéries deviennent insensibles aux substances censées les éradiquer, constitue une parfaite illustration de la sélection naturelle si chère à Darwin. Quand un antibiotique est appliqué sur une population bactérienne, inévitablement très diverse génétiquement, il se trouve bien souvent quelques bactéries naturellement armées pour déjouer l’attaque (par exemple en produisant une enzyme qui modifie, dégrade l’antibiotique ou qui présente des modifications de la cible de l’antibiotique). Ces bactéries résistantes, seules rescapées, deviendront alors la norme et transmettront les gènes responsables de cette résistance à leurs descendantes. Mais ces microorganismes ont un atout crucial supplémentaire : les plasmides, de petits fragments d’ADN circulaire totalement indépendants du reste du génome bactérien. Ces plasmides portant parfois un gène de résistance vont pouvoir être dupliqués et transmis aux bactéries voisines. Et ce, même si lesdites bactéries appartiennent à une autre souche, voire à une autre espèce.
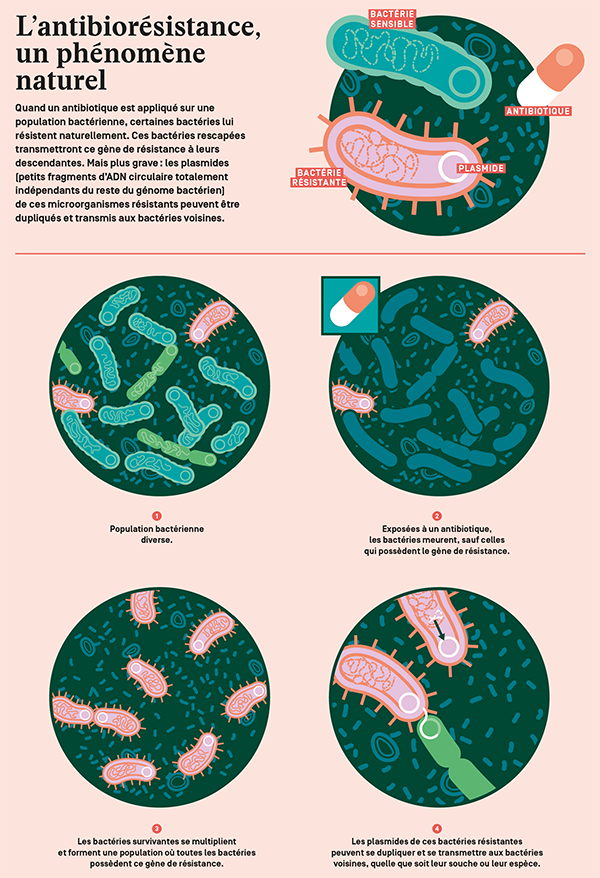
Des bactéries résistantes et sans frontières
Les exemples de transmissions d’une espèce à une autre sont nombreux. Les résistances acquises par les bactéries présentes dans les animaux d’élevage par exemple, peuvent se transmettre aux bactéries de notre microbiote intestinal. Chez les éleveurs au contact de leurs bêtes bien sûr, mais aussi par la manipulation et la consommation de produits animaux (viande, lait, œufs…). Des études ont également montré qu’au sein d’un même foyer, les bactéries des animaux de compagnie et de leurs propriétaires pouvaient partager les mêmes gènes de résistance.
Le compartiment « environnement » du triptyque « une seule santé » n’est pas non plus en reste. D’une part des résistances peuvent apparaître naturellement dans les bactéries du sol ou de l’eau, et potentiellement se transmettre à l’homme et l’animal. D’autre part, ces bactéries ou gènes résistants sont relâchés dans l’environnement, comme les antibiotiques, via les eaux usées pour l’homme ou l’épandage de lisier pour les animaux d’élevage. De 2017 à 2020, le projet MadSludge a ainsi passé en revue les meilleures méthodes pour limiter le transfert de résistances dans l’environnement via les rejets de stations d’épuration. « Avec l’antibiorésistance, il est certain que les transferts sont multiples entre les trois compartiments – homme, animal, environnement –, les incertitudes aujourd’hui ne concernent que la proportion de chaque compartiment », résume Alain Bousquet-Mélou, directeur de l’unité mixte INRAE/ENVT InTheRes, très impliquée dans ces recherches, y compris dans le projet MadSludge.
Une prise de conscience récente
Pendant des décennies, la montée de l’antibiorésistance n’a pas inquiété grand monde. Telle bactérie acquérait une résistance à la pénicilline ? Le médecin ou le vétérinaire se tournait vers une autre molécule… jusqu’à ce que la bactérie en question devienne résistante aux deux antibiotiques. Une prise de conscience mondiale apparaît à l’aube du xxi e siècle, lorsque la médecine se trouve de plus en plus fréquemment confrontée à des maladies multirésistantes, jusqu’à l’impasse thérapeutique (lorsque des bactéries s’avèrent résistantes à tous les antibiotiques connus). De quoi faire craindre à l’OMS « une ère post-antibiotique dans laquelle des infections courantes et de petites blessures seront à nouveau mortelles ». L’organisation mondiale présente désormais l’antibiorésistance comme « l’une des plus graves menaces pesant sur la santé mondiale ».
La baisse de l’usage est la solution

Pour enrayer sa progression, un seul mot d’ordre : limiter au maximum l’utilisation d’antibiotiques, et ce, dans tous les secteurs. Côté médecine humaine, les pouvoirs publics français lancent dès 2002 le slogan « les antibiotiques, c’est pas automatique ». D’autres campagnes s’adresseront par la suite aux médecins de ville, au personnel hospitalier, aux pharmaciens, etc. Côté santé animale, l’État français lance en 2012 le plan Écoantibio, qui vise une réduction de la consommation d’antibiotiques en élevage de 25 % en l’espace de 5 ans. Un succès, la baisse atteignant 37 % dans ce laps de temps.
Un an plus tard, INRAE lançait de son côté un Réseau recherche antibiotiques animal (ou R2A2) pour mettre en relation les acteurs impliqués et réfléchir ensemble à des stratégies de réduction. « R2A2 a réuni jusqu’à 250 personnes, majoritairement d’INRAE mais pas uniquement. Nos réunions d’échanges attiraient aussi des vétérinaires, des instituts privés, des industriels, des enseignants techniques agricoles… », raconte Christian Ducrot, directeur de recherche INRAE aux manettes de ce réseau. « Cela a permis que des gens se rencontrent, réfléchissent à des solutions, puis montent des projets ensemble. »
Parmi les nombreux projets nés du réseau R2A2, on peut citer ROADMAP, réunissant 17 partenaires et 10 pays entre 2019 et 2023 avec un budget de 6 millions d’euros. « L’idée était d’analyser la situation de l’antibiorésistance et trouver des leviers de changement des pratiques dans un esprit très interdisciplinaire, avec de l’économie, de l’épidémiologie, des sciences participatives, le tout guidé par les sciences humaines et sociales », raconte le porteur du projet, Nicolas Fortané.
Ce chercheur en sociologie à INRAE est également à l’origine d’AMAGRI, un projet de recherche devenu aujourd’hui un collectif qui tente de trouver les réponses à plusieurs questions sociologiques liées à l’antibiorésistance. « Le problème est connu depuis longtemps, alors pourquoi a-t-on agi aussi tardivement ? Quels sont les enjeux qui conditionnent les changements de pratiques ? Quels sont les fondements économiques, professionnels et politiques de notre modèle de régulation des antibiotiques ? ».
Les alternatives aux antibiotiques
Pour réduire concrètement l’utilisation d’antibiotiques en élevage, plusieurs stratégies sont étudiées. Tout d’abord, mieux comprendre certaines pathologies dans les élevages et développer d’autres traitements (vaccins, probiotiques, huiles essentielles…). « En marge des stratégies de substitution, il y a aussi une grande marge d’amélioration de l’antibiothérapie : en associant plusieurs médicaments, en diminuant la durée de traitement ou encore en optimisant les modalités d’administration, on peut réduire les quantités d’antibiotiques utilisées et donc les risques de voir apparaître des résistances », détaille Alain Bousquet-Mélou. L’unité InTheRes qu’il dirige, créée en 2018, cherche également à développer des alternatives à la métaphylaxie. Autrement dit, le fait de traiter en masse tout un élevage dès l’apparition de quelques individus malades, une démarche préventive et curative de plus en plus questionnée.
Pour cela, InTheRes développe des outils basés sur l’intelligence artificielle pour surveiller les animaux. Par exemple, des capteurs embarqués sur le bétail qui suivent en continu leurs déplacements, leur alimentation ou leurs comportements. Le but : repérer dès les premiers signes un animal malade pour le soigner avant qu’il ne contamine ses congénères. Une approche similaire est à l’essai dans les élevages de volaille, avec des caméras capables de suivre et d’identifier chaque animal présent à l’image, là aussi pour détecter précocement des animaux malades.
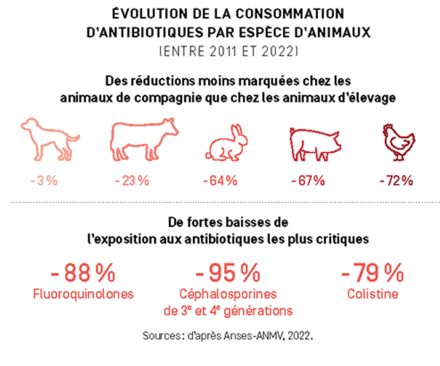
Alors que les plans Écoantibio 1 et 2 ont permis de diviser par deux l’exposition aux antibiotiques entre 2011 et 2022, le pari sera plus complexe pour le plan Écoantibio 3, lancé en 2024. « Nous avons commencé par nous attaquer aux usages excessifs d’antibiotiques, facilement évitables. Pour poursuivre cette baisse, les actions à entreprendre sont maintenant bien plus complexes, avec des changements en profondeur », admet Christian Ducrot. Mais surtout, la démarche devra être globale : dans tous les secteurs – médecins et vétérinaires travaillant de concert – et dans tous les pays. Or, si l’Union européenne a interdit dès 2006 l’utilisation d’antibiotiques comme facteurs de croissance, Chine, Brésil ou encore États-Unis de les utiliser en masse à cet effet, contribuant à la progression de l’antibiorésistance dans le monde.
Génétique et alimentation contre l’antibiorésistance
Lutter contre l’antibiorésistance dans l’élevage est un défi majeur pour préserver la santé animale et humaine. La baisse de l’usage des antibiotiques est donc essentielle. Edwige Quillet, cheffe du département Génétique animale (GA) d’INRAE, souligne aussi l’importance de la sélection génétique comme stratégie prometteuse : en choisissant des animaux plus résistants à certaines maladies, on réduit la nécessité d’utiliser des antibiotiques. Par exemple, chez les ruminants laitiers, la sélection pour la résistance aux mammites (inflammations de la mamelle, provoquées essentiellement par des bactéries) permet d’améliorer leur longévité tout en diminuant le recours aux traitements antibiotiques. De même, chez les poissons, des travaux de sélection contre certaines bactérioses ont été entrepris, permettant une réduction de l’usage des antibiotiques dans les élevages aquacoles. Adopter une approche systématique, intégrant mesures curatives et préventives, est nécessaire pour combattre efficacement l’antibiorésistance. Les recherches explorent d’autres pistes comme des systèmes de pâturage qui mélangent bovins et petits ruminants. Ce qui permet aux bovins, moins sensibles, d’ingérer les larves parasitaires, contribuant ainsi à réduire la pression pathogène globale ou encore leur alimentation.
-
Yann Chavance
(Envoyer un courriel)
Rédacteur
