Quel est l’impact du transfert du microbiote maternel sur la santé de l’enfant en particulier sur le risque d’obésité ?
Publié le 09 novembre 2022

L’idée que l’alimentation de la mère et son état métabolique peuvent notablement influencer la santé de sa descendance, en agissant en premier lieu sur la croissance fœtale puis en créant un terrain favorable à la santé ou à l’émergence de maladies métaboliques, est apparue à la fin des années 90. Le concept de l’origine développementale de la santé et des maladies (DOHaD) a été confirmé par un grand nombre d’études expérimentales sur des modèles animaux et élargi à de nombreuses pathologies. Il a, en particulier, été montré que l’alimentation des parents (et des grands parents) et leur état métabolique orientent la physiologie et le comportement alimentaire de la descendance Depuis ces travaux, un nouvel acteur incontournable est apparu : le microbiote, et une question fondamentale : quel est l’impact du transfert du microbiote (de la mère au petit) sur la santé de l’enfant ?
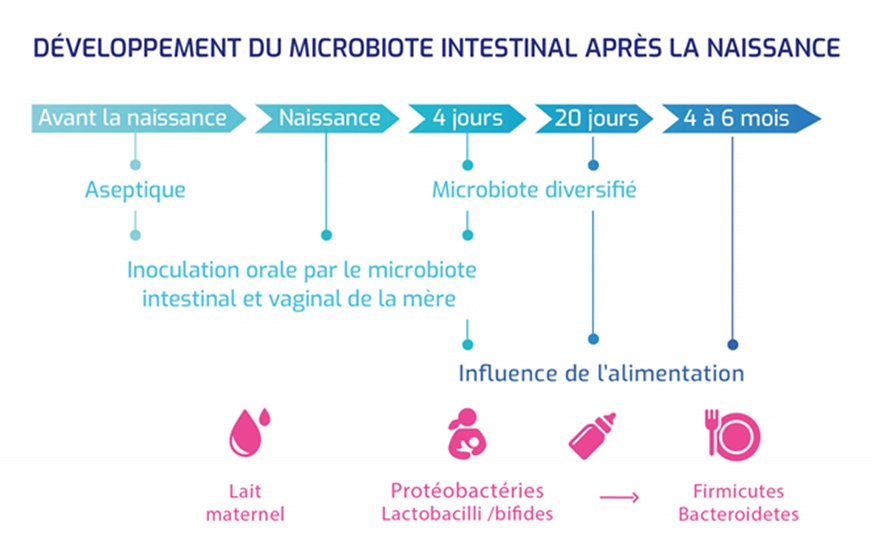
Le microbiote intestinal relai ou mémoire de la santé des parents joue-t-il un rôle dans l’origine développementale de la santé et des maladies de l’enfant ?
Si oui, comment le microbiote transféré de la mère à l’enfant agit pour influencer le comportement alimentaire de celui-ci ?
Pour développer des stratégies de prévention de l'obésité infantile, il vaut mieux en comprendre les causes. Conformément au concept du DOHaD, la littérature suggère que la transmission du risque d’obésité de la mère vers l’enfant ne résulterait pas de la seule prédisposition génétique. La transmission d'un microbiote « signature » de l'obésité maternelle à son enfant au cours du développement périnatal pourrait modifier le développement des structures cérébrales responsables de la régulation de la prise alimentaire et ainsi modifier l’appétit au cours de la vie.
L’équipe de recherche PhAN a émis cette hypothèse sur la base des constats suivants :
1) dans des modèles animaux, l'obésité maternelle peut influencer le neurodéveloppement en période périnatale avec des conséquences sur les structures cérébrales qui régulent l'appétit,
2) la composition des microbiotes maternels diffère selon le statut pondéral,
3) les microbiotes maternels sont les principaux déterminants de la colonisation de l'intestin de l'enfant,
et 4) le microbiote intestinal peut interagir avec le développement cérébral.
Pour tester le seul rôle de la composition microbienne maternelle, un transfert du microbiote (microbiote intestinal, vaginal ou du lait maternel) de mères génétiquement prédisposées ou non à l'obésité et nourries avec un régime hyper-énergétique, a été réalisé chez des rats nouveau-nés.
En accord avec l’hypothèse des compositions bactériennes différentes ont été identifiés partir des matières fécales et du lait de rattes, selon qu’elles étaient obèses ou minces malgré la consommation d’un régime obésogène. Donnés aux ratons nouveau-nés ces microbiotes modifiaient seulement transitoirement la composition de leur microbiote intestinal mais changeaient durablement les caractéristiques de leur comportement alimentaire. Quand le microbiote transféré provenait des mères obèses la descendance consommait plus de lait jusqu’au sevrage et plus de croquettes aux différentes périodes de leur vie d’adulte. A la recherche de mécanismes quelques espèces bactériennes différentiellement abondantes chez les ratons au moment du sevrage ont été identifiées et des tests supplémentaires vont permettre de rechercher, sur les espèces cultivables, si elles sont responsables du phénotype comportemental observé.
Quelles sont les perspectives ?
Ce projet a permis d’identifier le microbiote maternel en tant que canal de communication / transmission entre la mère et sa descendance. Plusieurs types de biomarqueurs pourraient expliquer les changements comportementaux, comme des espèces bactériennes transmises de la mère au petit ou des métabolites bactériens identifiés dans le plasma ou les contenus intestinaux de la descendance. Il faut encore comprendre comment le microbiote affecte le comportement alimentaire de la descendance en caractérisant son impact sur le neurodéveloppement des structures cérébrales des petits.
PARTENAIRES SCIENTIFIQUES :
Christine Heberden, UMR Micalis
Emmanuelle Lechatelier Metagenopolis
FINANCEMENT : ANR-16-CE14-0003-01
PUBLICATION ASSOCIEE :
Anne-Lise Pocheron, Gwenola Le Drean, Helene Billard, Thomas Moyon, Anthony Pagniez, Christine Heberden, Emmanuelle Le Chatelier, Dominique Darmaun, Catherine Michel, Patricia Parnet. Maternal Microbiota Transfer Programs Offspring Eating Behavior. Frontiers in Microbiology, 12, https://dx.doi.org/10.3389/fmicb.2021.672224, https://hal.inrae.fr/hal-03271317
