Alimentation, santé globale 5 min
L’intelligence artificielle au service de la santé animale
Les recherches à l’interface entre Santé Animale et Intelligence Artificielle sont en plein essor. Des chercheurs d’INRAE ont réalisé une étude bibliométrique sur 110 publications internationales, ainsi qu’une enquête auprès des équipes concernées au sein d’INRAE, afin de dégager les progrès réalisés, mais aussi les verrous méthodologiques et les défis de demain. Entretien avec Pauline Ezanno, épidémiologiste et spécialiste de la modélisation en santé animale.
Publié le 15 avril 2021

« Deep learning », « machine learning », « algorithmes apprenants », l’intelligence artificielle (IA) développe un grand éventail d’approches pour soutenir la réflexion humaine quand ses capacités d’abstraction ou de traitement de données sont dépassées. Plutôt que d’entrer dans la complexité des méthodologies, Pauline Ezanno délivre quelques messages importants à propos de l’IA, parmi lesquels la nécessité de travailler de manière transdisciplinaire, le besoin de temps et l’importance cruciale des données.
En quoi consiste l’intelligence artificielle appliquée à la santé animale ?
L’analyse d'une épidémie a posteriori est très intéressante pour progresser
Pauline Ezanno : L’intelligence artificielle (IA), dans son acception la plus large, combine des méthodes issues des mathématiques, des statistiques et de l’informatique. L’IA regroupe un ensemble de méthodes pour aider l’esprit humain à appréhender des systèmes complexes, les modéliser, élaborer et comparer des scénarios et des stratégies pour résoudre un problème, de la manière la plus automatique possible. Prenons un exemple. Dans mon équipe, nous travaillons sur la propagation et la maîtrise de maladies animales infectieuses. Typiquement, une épidémie est un de ces systèmes complexes, avec des paramètres qui peuvent évoluer dans le temps. Souvent, la modélisation mathématique est mobilisée pour contribuer à mieux comprendre une épidémie et à anticiper sa dynamique. Cependant, on l’a bien vu avec la Covid19, c’est très compliqué de suivre la propagation d’une épidémie en temps réel, quand il y a en plus des évènements qui viennent se greffer comme l’apparition de nouveaux variants du virus. De plus, il est difficile de travailler sous pression, alors qu’en réalité, il faut beaucoup de temps pour réunir les données, les analyser, développer des modèles suffisamment réalistes pour pouvoir comparer des scénarios, mais suffisamment simples pour répondre vite à la demande. Il faut aussi du temps pour mettre les modèles à jour lorsqu’il y a des changements ou de nouvelles connaissances à intégrer. De ce point de vue, l’analyse « a posteriori » est très intéressante pour progresser : on peut en effet comparer les modèles qui ont été développés et en tirer des enseignements. Des « challenges de modélisation » peuvent être réalisés après coup comme ce fut le cas pour Ebola, la dengue ou le chikungunya. Dans le cas de la fièvre aphteuse, on continue à analyser les données et à travailler sur les modèles vingt ans après l’épidémie de 2001 au Royaume-Uni. Mais cela vient après la crise. Pour faire de la prédiction « en temps réel », il faudrait « apprendre » aux modèles mathématiques à se mettre à jour automatiquement quand arrivent de nouvelles données, ce qui représente encore un défi méthodologique que l’IA pourrait relever.
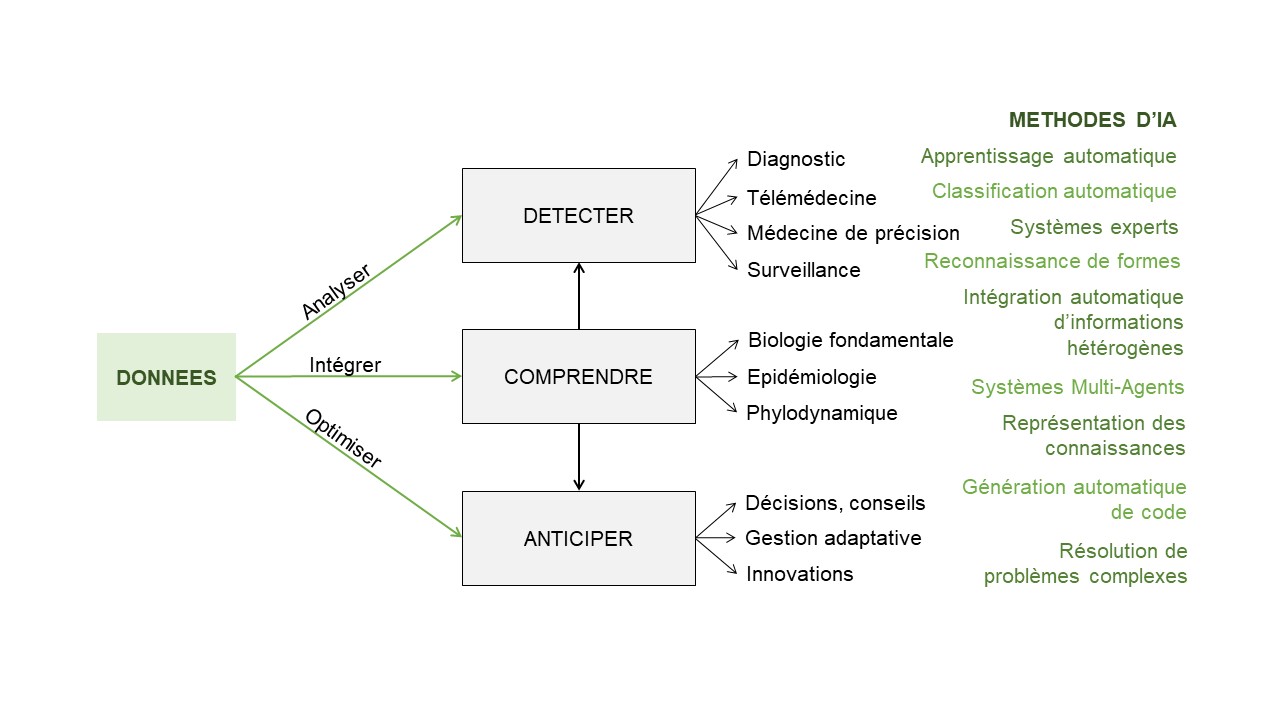
Outre le suivi des épidémies, l’IA peut avoir de nombreuses autres applications en santé animale, entre autres : détecter l’émergence d’une maladie (en recherchant des alertes par fouille de texte sur le web, en analysant des données collectées en routine en élevage, etc.) ou encore diagnostiquer automatiquement des maladies (par « reconnaissance de formes », c’est-à-dire reconnaissance d’anomalies types).
Pouvez-vous nous donner quelques exemples concrets d’application de l’IA à la santé animale ?
P. E. : Pour prendre des exemples au sein de notre équipe, nous avons développé le logiciel IVAN avec la chaire de télémédecine d’Oniris pour aider les vétérinaires à identifier les causes de la mort d’un animal à partir de son autopsie. Ce logiciel autoapprenant, construit à partir d’une base de données, guide le vétérinaire dans la réalisation de l’autopsie : en fonction des données renseignées par le vétérinaire, le logiciel indique quel organe regarder et quelles sont les hypothèses de diagnostic, avec les marges d’erreur. La chaire a aussi développé des lunettes connectées à une caméra (projet Dexter-e-T), qui permettent à une experte en autopsie d’être contactée par les vétérinaires à distance et de « voir » ce qu’ils voient, afin de réaliser une « télé-expertise ».
Générer automatiquement des modèles à partir de descriptions
Un autre logiciel, EMULSION, développé aussi dans notre équipe, mobilise deux approches d’IA : représentation des connaissances et système multi-agents multi-niveaux. Il génère automatiquement le code informatique d’un modèle épidémiologique à partir de sa description sous forme de texte structuré. Ce générateur de modèle facilite les interactions avec les non modélisateurs (gestionnaires de la santé, biologistes, etc.) car tout le contenu du modèle est lisible et modifiable facilement, évitant l’effet « boîte noire » souvent reproché aux modèles par leurs utilisateurs finaux. Cette technologie a été éprouvée pour des épidémies locales (dans une population) ou se propageant sur des réseaux de mouvements (dans une région). Les travaux en cours visent maintenant à représenter explicitement l’espace géographique, même à très large échelle. Une telle approche contribuera aussi à constituer des « bibliothèques » de modèles types, pour s’adapter plus rapidement à de nouvelles émergences, car il en survient chaque année qui diffèrent des précédentes.
Générer automatiquement des outils d’aide à la décision à partir des modèles
Nous avons enfin une autre innovation très prometteuse en cours (projet ATOM) qui permet cette fois de générer automatiquement des outils d’aide à la décision (OAD) à partir des modèles. Nous avions déjà proposé dès 2015 aux gestionnaires de la santé animale des outils d’aide à la décision pour raisonner les interventions sanitaires en élevage pour gérer la diarrhée virale bovine (EvalBVD) et la paratuberculose (EvalParaTuB). Cependant, le temps de développement de ces OAD est conséquent. Dès l’année prochaine, ATOM fournira des OAD aux vétérinaires sans délai après le développement et l’analyse des modèles sous-jacents.
Comment s’assurer de l’accès aux données ?
P. E. : Les données sont en effet un point central. Les données observées, dans leur diversité, sont mobilisées en amont pour l’élaboration des méthodologies d’IA. Les données accumulées permettent aussi de s’assurer en aval de la validité des modèles et de leur permettre de s’autocorriger, par exemple selon des processus d’apprentissage automatique (machine learning). Mais il faut rester conscient que même les modèles les plus performants, comme par exemple les modèles météorologiques, alimentés par des millions de données, restent des approximations de la réalité, avec des marges d’erreur : on ne peut pas prévoir la météo avec une certitude totale, mais il est possible de la prédire avec un degré défini d’incertitude.
En santé animale, les données sont de natures très diverses : elles peuvent être collectées automatiquement sur les animaux, via des capteurs, ou enregistrées réglementairement (mouvements commerciaux, plateforme d’épidémiosurveillance), ou encore elles peuvent être d’origine privée (collecte de lait par exemple). Il faut aussi s’assurer que ces données sont comparables, on parle « d’interopérabilité ». Il est donc crucial d’organiser le dépôt et la protection des données au niveau national, à l’échelle interinstitutionnelle, et pour cela, la plateforme ESA est un lieu privilégié. Lire l’article. Certaines données, comme celles du métabolome ou de l’épigénétique, constituent un nouvel enjeu.
En conclusion ?
Il faut beaucoup de temps et de cerveaux !
P. E. : L’IA appliquée à la santé animale est une activité d’interface qui mobilise de nombreuses disciplines : épidémiologie, infectiologie, immunologie, génétique, écologie, évolution, sciences cliniques… en plus des disciplines mathématiques, statistique et informatique. Il est donc très important de favoriser les interactions au sein d’équipes transversales, encouragées par des financements incitatifs interinstitutionnels qui acceptent des prises de risques… De plus, pour que les utilisateurs finaux (vétérinaires, éleveurs) s’approprient les outils d’aide à la décision générés, il faut développer la formation, initiale et continue, afin de dépasser les réticences liées à la complexité des outils ou à la crainte qu’ils ne remplacent l’expertise humaine, ce qui n’est pas le cas. On peut aussi s’attacher à rendre plus transparents les systèmes et approches informatiques, et privilégier la co-construction des outils avec leurs utilisateurs dans des projets de science participative. En résumé, nous progressons de manière continue, mais il faut beaucoup de temps et beaucoup de « cerveaux » !
Références :
- Ezanno et al. 2021. Vet Res 52:40. https://doi.org/10.1186/s13567-021-00902-4
- Ezanno P., Picault S., Winter N., Beaunée G., Monod H., Guégan J-F. 2020. Intelligence artificielle et santé animale. INRAE Prod. Anim., 33, 95-108. https://doi.org/10.20870/productions-animales.2020.33.2.3572
- Picault S., Huang Y.-L., Sicard V., Arnoux S., Beaunée G., Ezanno P. 2019. EMULSION: transparent and flexible multiscale stochastic models in human, animal and plant epidemiology. PLoS Comput. Biol. 15 (9): e1007342, https://doi.org/10.1371/journal.pcbi.1007342
